【导读】
中老年男性,PET/CT诊断为“下丘脑恶性肿瘤”,因担心手术风险而选择立体定向放射治疗。治疗后病情短暂稳定,后继续进展,肿瘤进行性增大。之后行内镜下扩大经鼻入路手术,部分切除肿瘤,术后病理证实为颅咽管瘤。术后反复出现发热症状,最终诊断为下丘脑综合征(下丘脑性肥胖、脂肪肝、垂体前后叶功能减退、下丘脑性发热)。本病例主要探讨:颅咽管瘤如何诊断?颅咽管瘤的治疗有哪些争议和难点?颅咽管瘤患者的远期预后及生存质量如何?
【病例简介】
患者,男,61岁。因“伽马刀治疗下丘脑占位后1年,视力下降、嗜睡伴幻觉1天”于2015年9月入住华山医院神经外科。患者自2014年4月起无明显诱因下出现头痛、事物模糊伴嗜睡,症状呈进行性加重。于2014年8月至外院就诊,行MRI检查提示“下丘脑占位”,病灶最大径约20.3mm。2014年10月复查MRI示鞍上占位约35mm×24mm×27mm,较前增大。随后患者出现发热症状,最高体温38℃,伴多饮、多尿、大便干结、食欲减退,至华山医院内分泌科就诊,诊断为“垂体前叶功能减退(肾上腺皮质轴、甲状腺轴、生长激素轴、性腺轴)伴部分中枢性尿崩症”,给予肾上腺皮质激素和甲状腺激素替代治疗,病情有所缓解。建议穿刺活检以明确病灶性质,但患者及家属因惧怕手术风险未予采纳。出院后至外院行PET/CT检查,结果提示“鞍上见一不规则混杂低密度占位,放射性摄取异常增高,摄取范围约27mm×19mm×15mm,SUV最大值为10.8”,影像诊断考虑为“颅内原发性恶性肿瘤”。于外院行立体定向放射外科治疗(中心剂量20Gy,周边剂量8Gy)。治疗后患者自觉视力明显改善。2015年1月在外院复查MRI,结果提示病灶变化不明显。
2015年9月患者再次出现视力下降,嗜睡伴幻觉,入住华山医院神经外科。
现用药:双歧杆菌三联活菌胶囊,曲安奈德益康唑乳膏,左甲状腺素钠片,奥美拉唑肠溶胶囊,醋酸可的松片。
体格检查:体温36.4℃,脉搏84次/分,呼吸20次/分,血压114/82mmHg,身高174cm,体重92kg,步态不稳,轻度嗜睡,心、肺、腹查体无特殊。
【实验室及辅助检查】
生化检查:肝功能:ALT 245U/L↑,AST 85U/L↑;脂代谢:TC 7.99mmol/L↑,TG 9.97mmol/L↑,HDL-C 0.78mmol/L↓,LDL-C 1.73mmol/L。
垂体内分泌检查:晨血皮质醇0.43μg/dl;性腺轴激素:E2 18.40pmol/L,P 0.10nmol/L,FSH 0.10IU/L,LH 0.56IU/L,T 0.09nmol/L↓;PRL 23.01ng/ml↑。IGF-1 84.40μg/L;甲状腺轴激素:TSH 0.3860mIU/L↓,TT3 1.17nmol/L↓,TT4 67.50nmol/L,FT3 3.15pmol/L↓,FT4 10.34pmol/L↓。
鞍区增强MRI:鞍上池内见异常信号肿块影,T1WI等低信号,欠均匀。增强后不均匀强化。病灶大小约20mm×35mm×34mm。垂体未见明显受压,垂体柄居中,鞍底未见明显塌陷,垂体信号均匀,增强后未见明显异常强化灶(图1A~B)。
头颅CT:鞍区未见明显钙化(图1C)。
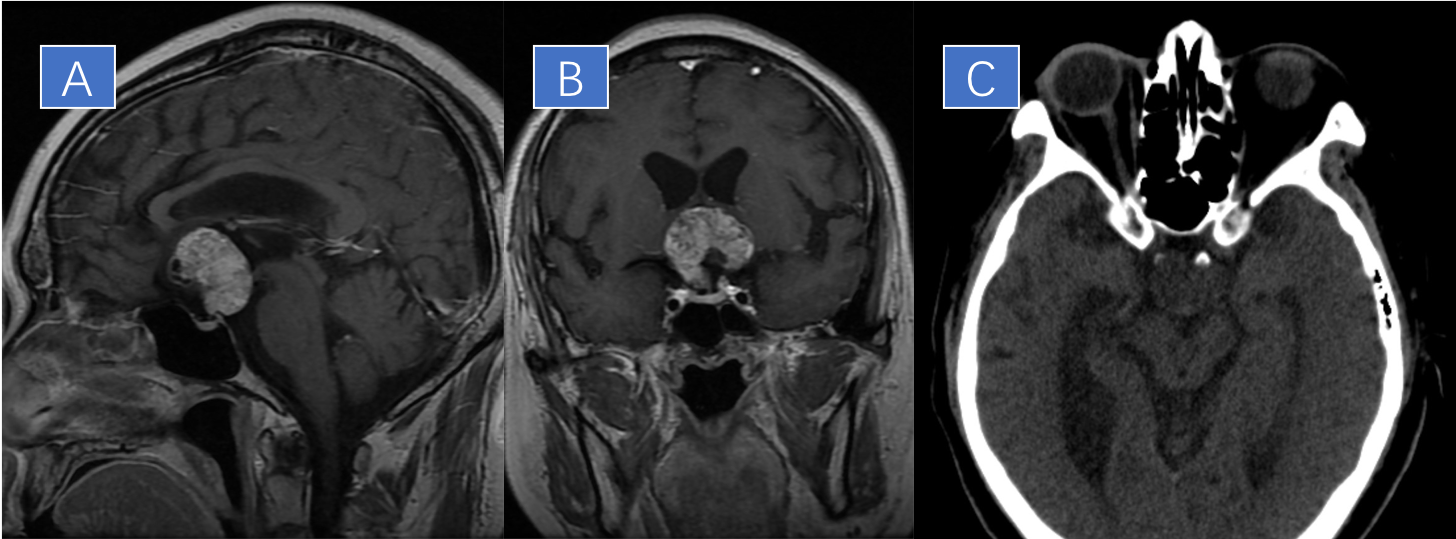
图1术前MRI及CT增强表现
A.矢状位,可见瘤体明显不均匀强化,垂体未见明显受压,鞍底未见明显塌陷,垂体信号均匀,增强后未见明显异常强化灶;B.冠状位,可见瘤体明显不均匀强化;C.头颅CT示鞍区未见明显钙化灶
【诊治经过1】
经内分泌评估,患者存在:①垂体前叶功能减退(肾上腺皮质轴、甲状腺轴、生长激素轴、性腺轴);②部分中枢性尿崩症。继续给予口服激素替代治疗:醋酸可的松早25mg、下午25mg,左甲状腺素钠50μg(每日1次),B超排除前列腺肿瘤后予十一酸睾酮胶丸40mg(每日2次),醋酸去氨加压素片每晚50μg。
下丘脑占位病灶经立体定向放射治疗后,目前仍有增大趋势,病因不明,提交MDT讨论对策。
【MDT讨论与临床决策】
问题:该患者下丘脑占位病灶性质如何?如果采取手术治疗,围术期该如何处理?
影像科意见:结合患者的病史以及本次影像学表现,考虑为颅咽管瘤可能性大,生殖细胞性肿瘤不除外,建议外科手术明确性质。
内分泌科意见:患者经内分泌评估,存在垂体前叶功能减退以及部分中枢性尿崩症,目前已接受激素替代治疗,病情部分缓解。但病灶体积呈进行性增大,内科保守治疗和立体定向放射治疗不能缓解其占位效应。建议手术治疗,明确病因并争取切除病灶。围术期糖皮质激素替代治疗剂量加大至应激剂量,注意维持水电解质平衡。
神经外科意见:患者目前存在垂体前叶功能减退、中枢性尿崩和明显的视神经受压症状。垂体前叶功能减退和中枢性尿崩症经内科治疗后,病情有所缓解,但视神经受压唯有采用外科手段干预。考虑到患者曾接受放射治疗,可能造成瘢痕粘连、肿瘤质地变硬、解剖层次不清等困难,且瘤体已累及下丘脑,过于激进的手术方案可能造成严重的并发症,甚至增加死亡风险。故手术计划以解除视神经受压作为主要目标,在尽可能安全的前提下对肿瘤行大部切除,尽可能减少对下丘脑功能的损伤。
临床综合分析与决策:通过反复沟通使患方充分理解并接受手术风险。内镜下行扩大经鼻入路鞍上肿瘤切除术。围术期注意水电解质平衡,糖皮质激素替代采用应激剂量。
【诊治经过2】
患者于2015年12月8日全麻下行内镜下扩大经鼻入路鞍上肿瘤切除术,术中见囊壁有钙化,和视交叉、垂体柄粘连,肿瘤发源于垂体柄下端,血供不丰富,术中采取分块切除的策略,部分肿瘤极其坚韧,和视交叉粘连紧密,未强行切除,最终达大部切除。术后复查MRI示肿瘤少许残留(图3)。术后病理示颅咽管瘤(乳头型)(图4、图5)。患者于2015年12月17日出院,出院时患者自觉双眼视力、视野较术前有改善,嗜睡和幻觉症状消失。
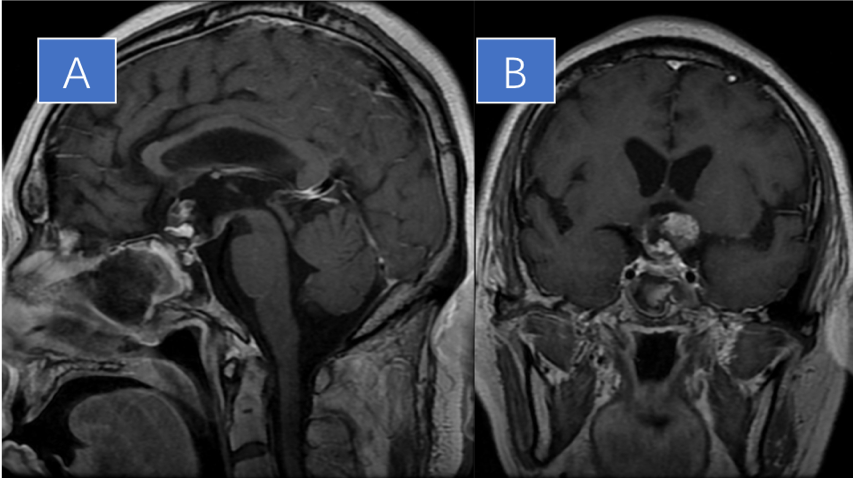
图3 术后MRI增强可见瘤体较术前明显缩小
A.矢状位;B.冠状位
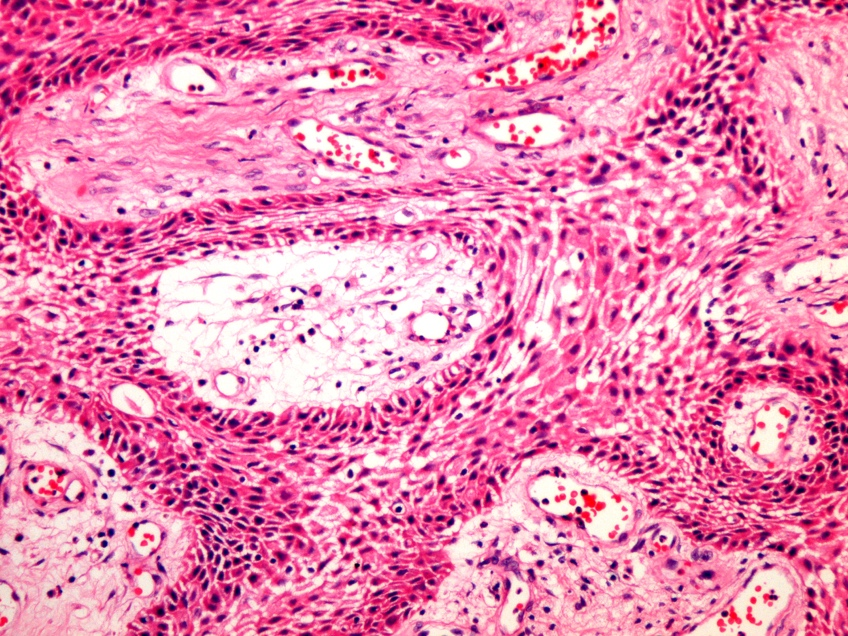
图4 术后病理示颅咽管瘤(乳头型)
鳞状上皮细胞围绕纤维血管轴心形成乳头状结构 (HE ×400)
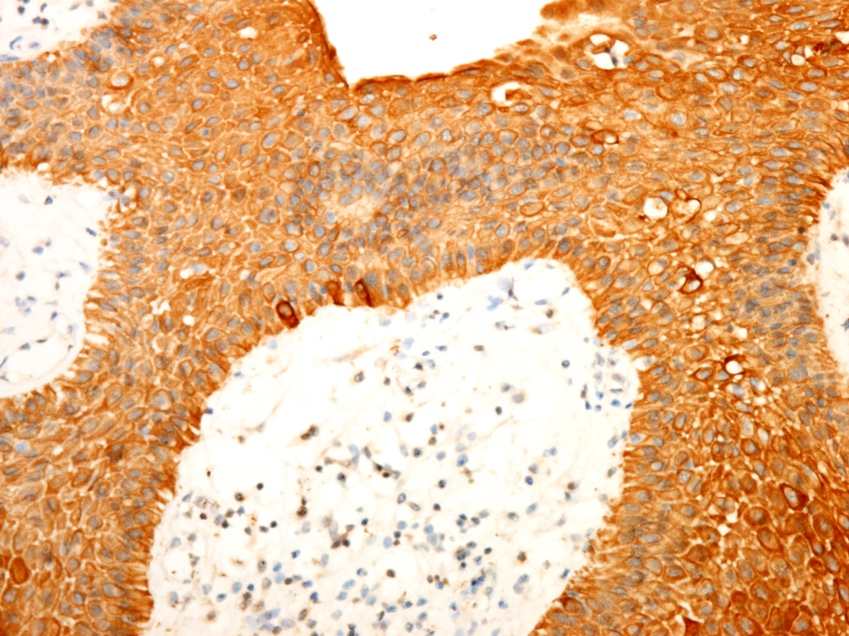
图5 术后病理免疫组化
瘤细胞CK阳性 (免疫组化法 ×400)
【随访与转归】
患者术后1个月内反复出现发热症状并于2016年1月28日再次入院。入院时患者无头痛,无脑脊液漏,无咳嗽、咳痰,无尿频、尿痛,无腹泻。查血常规:白细胞19.1×109/L,中性粒细胞百分比77.2%。C反应蛋白、降钙素原正常,肺部CT无感染证据。入院后体温波动于37~38℃,完善尿常规、血培养、腰椎穿刺等检查,同时经验性给予头孢哌酮-舒巴坦、哌拉西林-他唑巴坦等抗生素治疗,但体温无下降,之后各项检查结果未见感染证据。请抗生素科会诊,并经内分泌科讨论,结合病史考虑下丘脑性发热的可能性较大,诊断为下丘脑综合征(下丘脑性肥胖、脂肪肝、垂体前后叶功能减退、下丘脑性发热)。建议患者继续随访体温以及伴随症状,暂不予特殊处理。
在后续随访过程中,患者间或有低热症状,劳累后为重,但均未超过38℃,不伴有其他明显不适症状。定期行内分泌评估,调整激素替代剂量。患者自述食量增加,体重由75kg增加至90kg,BMI 29.7kg/m2。嘱患者低脂饮食,适量运动,并予非诺贝特降脂治疗。外院随访鞍区MRI未见残瘤增大。
【经验与体会】
(一)颅咽管瘤简介
颅咽管瘤是来源于颅咽管残余上皮细胞的一种少见的颅内肿瘤,可位于鞍上、鞍内或跨鞍生长,约占原发性颅内肿瘤的2%~5%,但在儿童原发性颅内肿瘤中占比高达15%。根据国外统计资料,其发病率约为0.13/10万,并且存在5~14岁和50~74岁两个发病高峰。颅咽管瘤在组织学上表现为良性,但是临床上也可能出现难以预料的生物学行为特点而造成严重的后果。常见的临床表现有头痛、视力下降和内分泌紊乱等。颅咽管瘤的病理分型主要为造釉细胞型和乳头型,其影像学表现与病理分型密切相关。造釉细胞型的颅咽管瘤主要发生于5~15岁的儿童,多为囊实混合性,绝大多数可在CT上发现钙化灶;而乳头型颅咽管瘤则主要发生于50岁以上的成人,CT上多不伴有钙化表现[1]。MRI检查对颅咽管瘤同样十分重要,由于其往往具有多囊性和钙化,T1WI和T2WI多表现为混合信号,T1增强可见强化的囊壁和实质性结构。根据病史、临床表现和典型的MRI和CT特征,多数颅咽管瘤的诊断较明确,但有时仍需与垂体瘤、鞍区脑膜瘤、视神经胶质瘤等鉴别。颅咽管瘤可选用的治疗手段包括手术和放射治疗,目前多主张首选手术治疗,若手术未能全切肿瘤,则对残余瘤体进行辅助放疗。
在治疗颅咽管瘤病灶的同时应评估垂体前、后叶功能,垂体功能减退者应给予相应的替代治疗。
(二)颅咽管瘤治疗的争议
在颅咽管瘤的治疗策略上目前主要存在两大争议。
争议点之一在于手术的切除程度。激进派的观点认为颅咽管瘤为良性肿瘤,除部分组织与视交叉、垂体柄、下丘脑和第三脑室等粘连外,其他区域与周围组织结构有胶质增生带或蛛网膜分界,应争取全切肿瘤,以减少复发,尤其是对于儿童患者。而保守派的观点则认为在有些情况下完全切除瘤体非常困难,比如瘤体直径大于4cm、钙化大于10%、与重要结构关系紧密等。过于激进的手术方案可能造成严重的并发症,甚至增加死亡风险。可行肿瘤部分切除或仅做囊肿穿刺抽液,再行放射治疗,不但手术风险明显降低,而且可以获得与肿瘤全切相似的长期预后[2]。本例中尽管已经采取了较保守的手术策略,但患者术后依然发生了下丘脑功能紊乱的表现,这也印证了手术对于下丘脑功能潜在的严重影响。因此,最大程度地切除肿瘤而不引起严重的并发症应该是颅咽管瘤手术治疗的合理策略。Müller[3]对儿童颅咽管瘤患者,根据术前下丘脑受累程度进行分级,对下丘脑受累严重的病例采取部分切除加放射治疗的策略,发现可以显著降低术后患儿发生肥胖的概率。
争议点之二在于放疗开始的时间。部分学者主张术后立即行放疗以延缓肿瘤进展;而另一些学者则主张先随访,当肿瘤进展时再行放疗,以减少不必要的放射性损伤。部分研究结果显示即刻放疗能显著减少肿瘤复发率。但同样有研究表明,采取随访策略的患者的整体生存期和无进展生存期与立即行放疗的患者相比无显著差异[4]。
我们期待有大样本的前瞻性随机对照临床试验,为上述争议性抉择提供依据。
(三)颅咽管瘤患者的远期预后和生存质量
颅咽管瘤患者常见的并发症包括视力受损、垂体前叶功能减退、尿崩症、食欲改变及肥胖相关性疾病,如糖尿病、高脂血症、高尿酸和脂肪肝等,另有行为异常、昼夜节律紊乱、体温调节失衡以及心率、血压不稳等较少见的并发症。这些因素综合起来可能会显著影响患者的生存和生活质量。本例患者就先后发生了视力减退、尿崩、垂体前叶功能减退、食欲改变、肥胖、代谢紊乱以及体温调节障碍等多种并发症,最终诊断为下丘脑综合征(下丘脑性肥胖、脂肪肝、垂体前后叶功能减退、下丘脑性发热)。
【专家点评】
颅咽管瘤是一种较为常见的颅内先天性肿瘤,可长在鞍内、鞍旁或鞍上,视交叉前方、后方、下丘脑、第三脑室内等部位。多数患者以视功能障碍、垂体前后叶功能减退起病,肿瘤巨大者可引起下丘脑功能障碍、颅高压、脑积水以及相邻脑叶受压引起的功能障碍,严重威胁病患的生命健康和生活质量。外科手术是治疗颅咽管瘤的首选方法,手术能否全切与下列因素有关:①儿童病人的肿瘤与周边正常组织粘连较少,全切后并发症较少,成人颅咽管瘤多与周围组织粘连紧密,全切后并发症多,致死、致残率高;②初次手术较复发后再次手术容易,全切除的机会较多;③临床上有明显的垂体、下丘脑功能障碍者,只适于做部分切除;④鞍内型及视交叉前型颅咽管瘤较易做全切除,视交叉后型及脑室型全切除机会少。因此,对于儿童病人、初次手术者、术前症状较轻者以及肿瘤位于有利解剖部位的患者,原则上应力争做到肿瘤全切除,以防止复发;而对于肿瘤与神经、血管、下丘脑粘连紧密者,或术前症状较重的患者,不宜强求全切除,宜部分切除肿瘤,对于有脑积水者争取打通脑脊液循环,术后辅以放射治疗。过去颅咽管瘤手术多采取经颅入路,因手术视野受到额叶、视交叉、大脑前动脉等结构的阻挡,暴露范围有限,手术风险较大,术后不良反应较多。近年来,随着神经内镜技术的不断发展,一些有条件的单位采用内镜下经鼻-蝶窦-鞍结节入路,可在直视下分离和切除肿瘤,保护重要的神经、血管、下丘脑结构,有利于提高手术全切除率、降低术后并发症发生率。术中对于下丘脑、视神经、视交叉、垂体柄及瘤周穿支血管的保护是有效降低术后并发症的重要前提。颅咽管瘤术后并发症以垂体前叶功能减退和水电解质紊乱最为常见,应行垂体前叶激素替代,密切监测、维持水电解质平衡,防治继发性损伤。
参考文献
[1] Müller HL. Craniopharyngioma. Endocr Rev, 2014, 35(3): 513-543.
[2] 周良辅. 现代神经外科学. 第2版. 上海: 复旦大学出版社, 2015: 739-747.
[3] Müller HL. Preoperative staging in childhood craniopharyngioma: standardization as a first step towards improved outcome. Endocrine,2016,51(1):1-3.
[4] Karavitaki N. Management of craniopharyngiomas. J Endocrinol Invest, 2014, 37(3): 219-228.
本文源于复旦大学附属华山医院《垂体疑难病多学科诊治病例精选》,主编叶红英,王镛斐。欲查看更多精选病例,请购买原书。